Команда исследователей из Сеченовского университета и Университета Питтсбурга, при участии научных коллективов из США и Португалии, раскрыла новые детали в работе иммунной системы, выявив различия в устойчивости клеток к ферроптозу — особому типу клеточной гибели. Оказалось, что тип активации макрофагов напрямую влияет на их жизнеспособность: клетки, участвующие в восстановлении тканей после воспаления, более подвержены разрушению, чем те, кто борется с инфекцией.
Сложность иммунных реакций и роль макрофагов
Когда организм сталкивается с повреждениями тканей, вирусами или бактериями, в действие вступает иммунная система. Ключевую роль здесь играют специальные клетки — макрофаги. Первые из них, М1-макрофаги или «солдаты», нацелены на борьбу с возбудителями и быстро удаляют разрушенные клетки. После того как острая фаза воспаления утихает, эстафету перенимают М2-макрофаги — «санитары», задача которых заключается в очищении тканей от остатков и их восстановлении. Слаженность в смене этих двух типов особенно важна: если «солдаты» задерживаются надолго, воспаление становится хроническим и несет вред организму.
Ферроптоз: механизм и его значение для здоровья
Ферроптоз — это специфическая форма гибели клеток, связанная с нарушением обмена железа и окислительным стрессом. С его помощью организм освобождается от дефектных и поврежденных клеток, поддерживая здоровый баланс в тканях и предотвращая развитие опухолей. Однако чрезмерная активность ферроптоза способна усилить воспалительный процесс, а недостаточная — помешать очищению организма от опасных клеток. Глубокое понимание этого типа клеточной гибели становится все более востребованным как для терапии хронических воспалений, так и для развития антираковой стратегии.
Неравная устойчивость макрофагов: важное открытие
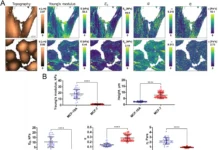
Исследования показали, что макрофаги разных типов реагируют на ферроптоз по-разному. «Солдаты» (М1) оказываются гораздо более устойчивыми, тогда как «санитары» (М2) страдают от этого механизма быстрее и сильнее. Такое открытие позволяет объяснить, почему иногда воспаление не переходит вовремя в стадию восстановления: клетки, которые должны обновлять и очищать ткани, исчезают быстрее, чем это необходимо. Более того, остатки разрушенных клеток поддерживают воспалительный процесс, создавая замкнутый круг.
Прогнозирование и контроль воспалительных процессов
В ходе работы были проведены многочисленные лабораторные эксперименты, результаты которых позволили построить математическую модель устойчивости различных типов макрофагов. Такой инструмент способен не только анализировать уже произошедшие события, но и прогнозировать течение воспаления в зависимости от баланса между М1- и М2-макрофагами. Это открывает новые горизонты в регулировании иммунных реакций и поиске эффективных способов борьбы с хроническими воспалениями и даже с опухолями.
Потенциальные перспективы для медицины
Данное исследование значительно продвинуло понимание тонких процессов, определяющих жизнеспособность и эффективность работы макрофагов. Новые знания дают ученым возможность создавать инновационные подходы для управления клеточной гибелью и воспалительными реакциями. В долгосрочной перспективе такие открытия несомненно приведут к созданию новых методов профилактики и лечения различных заболеваний, обеспечивая пациентам более быстрое восстановление и защиту от хронических недугов.
Изображение: логотип с сайта Сеченовского университета
Источник: scientificrussia.ru